Nombre sistemático: pruebas farmacogenéticas
Aspectos generales
¿Qué es la farmacogenética?
Cada individuo responde de una forma diferente ante un mismo medicamento, o puede presentar diferentes efectos secundarios. La manera en la que se responde puede deberse a los genes que se han heredado. Con respecto a los fármacos, la composición genética de cada persona y la respuesta individual puede significar que un medicamento que resulta eficaz para una persona puede ser menos eficaz para otra, o que un medicamento que es seguro para una persona puede serlo menos para otra, incluso utilizando la misma dosis.
La mayoría de los medicamentos se descomponen (metabolizan) en el organismo a través de diferentes enzimas. En algunos casos, un fármaco activo se hace inactivo (o menos activo) a través del metabolismo. En otros casos, un fármaco inactivo (o menos activo) se hace más activo a través del metabolismo. El reto en el tratamiento farmacológico es asegurarse de que la forma activa de un fármaco se queda el tiempo suficiente en el cuerpo para realizar sus funciones. Sin embargo, algunas personas tienen actividades enzimáticas diferentes, por lo que pueden metabolizar el fármaco demasiado rápido o demasiado lento, o incluso no hacerlo en absoluto, lo que significa que el medicamento puede no producir el efecto deseado o puede permanecer en el cuerpo de una persona durante mucho tiempo, produciendo efectos adversos.
La respuesta individual a un fármaco también puede estar relacionada con la variabilidad en la diana del medicamento, por ejemplo una proteína a la que el medicamento se une para producir un efecto específico. Además, las personas pueden presentar efectos adversos (conocidos como reacciones de hipersensibilidad) a ciertos medicamentos debido a la variabilidad en las proteínas implicadas en la respuesta inmune.
A menudo, los términos “farmacogenética” y “farmacogenómica” se utilizan indistintamente. Existen diferencias sutiles en el significado de ambos términos pero no existe un consenso acerca de las definiciones exactas. En general, la farmacogenómica se refiere al estudio general de todo el grupo de genes que contribuyen a la respuesta de un medicamento. La farmacogenética es el estudio y la evaluación de las diferencias heredadas (variaciones genéticas) que afectan al metabolismo de los fármacos y la respuesta de un individuo a los medicamentos. A efectos de este artículo, se utilizará el término farmacogenética.
Preguntas comunes
¿Por qué es importante la farmacogenética?
Cuando se inicia un tratamiento farmacológico para una determinada enfermedad, el médico recetará un fármaco eligiendo entre todos los que hay disponibles. Las dosis y los tiempos de administración se basan por lo general en el metabolismo y eliminación del fármaco medios de una persona estándar. Por lo tanto, se prescribe una dosis estándar en función de factores como el peso, el sexo y la edad. Sin embargo, en la práctica cada persona responde de una forma diferente al tratamiento, y el médico debe ajustar las dosis. Por ejemplo, el médico deberá reajustar la dosis o cambiar a un tratamiento distinto en función de si la persona responde al tratamiento o si presenta efectos secundarios adversos o peligrosos. En algunas ocasiones, una persona a la que un tratamiento le está funcionando correctamente, de repente al tomar un nuevo fármaco puede presentar signos o síntomas indeseables.
Las concentraciones o efectos de algunos fármacos pueden monitorizarse con pruebas en sangre y las dosis de los fármacos pueden aumentarse o reducirse para mantener los niveles dentro del rango terapéutico establecido. El seguimiento de la concentración del fármaco se conoce como monitorización de fármacos. Si el cambio en la dosis del fármaco no causa un efecto positivo en el tratamiento o control de la enfermedad, o la persona todavía presenta efectos secundarios, entonces deberá utilizarse un fármaco diferente.
Por el contrario, la farmacogenética ofrece a los médicos la oportunidad de individualizar el tratamiento farmacológico en función de las características genéticas de la persona. Realizar este tipo de pruebas antes de empezar un tratamiento para determinar la probabilidad de respuesta a diferentes tipos de medicamentos es un área con mucho futuro. Esta información genética podría ser útil en el momento de elegir un tratamiento farmacológico así como las dosis a administrar. Para algunos medicamentos, la farmacogenética ya es de gran ayuda para determinar los fármacos y dosis más adecuados para obtener el efecto deseado, al tiempo que se reduce la probabilidad de presentar efectos adversos.
¿Cómo varían los genes y cómo funcionan las pruebas farmacogenéticas?
Los genes son las unidades básicas de material genético. Se trata de fragmentos de ADN que normalmente codifican la producción de proteínas, incluyendo las proteínas conocidas como enzimas. Cada persona tiene dos copias de la mayoría de los genes: una copia heredada de la madre y la otra del padre. Cada gen se compone de un código genético específico, que es una secuencia de nucleótidos. En cada nucleótido puede haber una de las cuatro posibles bases nitrogenadas (A, T, G o C). Para cada posición de las bases nitrogenadas en el gen, una de ellas es la predominante en la población, y se conoce como “tipo salvaje”(wild type). Si un individuo tiene un nucleótido diferente del “tipo salvaje” en uno de sus alelos, se dice que ese individuo es heterocigoto. Si un individuo tiene el mismo nucleótido (salvaje o variante) en ambos alelos del gen, se dice que ese individuo es homocigoto.
Las variantes genéticas (también conocidas como polimorfismos o mutaciones) ocurren en toda la población. Algunas variantes genéticas son benignas y pueden estar asociadas a características como la altura, el color del cabello o de los ojos. Otras variantes genéticas pueden ser la causa de ciertas enfermedades. Además, existen variantes que condicionan la respuesta a determinados medicamentos.
Las pruebas farmacogenéticas buscan estas últimas. Estas variantes se encuentran en genes que codifican las enzimas metabolizadores de fármacos, dianas farmacológicas, o proteínas implicadas en la respuesta del sistema inmunitario. Las pruebas farmacogenéticas determinan además si las variantes se encuentran en heterocigosis o en homocigosis, lo que puede afectar la respuesta de un individuo a un fármaco concreto.
¿Cuándo se solicitan?
El médico puede solicitar este tipo de pruebas para localizar determinadas variantes que se sabe que están involucradas en la respuesta a un fármaco. El estudio se puede realizar en cualquier momento durante el tratamiento, ya sea antes del tratamiento, durante la fase inicial o en una fase más avanzada. Los resultados de las pruebas se evalúan en función de las características del paciente, como pueden ser la edad, el peso, el estado de salud y otra medicación que pueda estar tomando, para personalizar el tratamiento. En algunas ocasiones, el médico puede utilizar esta información para ajustar la dosis del fármaco o a veces para elegir un fármaco diferente. El objetivo de las pruebas farmacogenéticas es ofrecer una información adicional, pero no sustituye la necesidad de monitorización del fármaco.
Cada prueba farmacogenética sólo se realiza una vez en la vida, puesto que el material genético no se modifica a lo largo del tiempo. En función de la medicación a utilizar, pueden solicitarse pruebas farmacogenéticas para uno o varios genes. Un ejemplo de medicación para la cual generalmente se evalúan diferentes genes es la warfarina, puesto que puede estar afectada por variantes genéticas en el CYP2C9 y en el VKORC1.
Las pruebas pueden realizarse antes de empezar el tratamiento con un fármaco específico o si un individuo que ha empezado un determinado tratamiento presenta efectos secundarios o dificultades para establecer o mantener una dosis estable. En algunas ocasiones, sólo se dan estas situaciones cuando se añaden o retiran otros medicamentos que afectan el metabolismo del fármaco en cuestión.
¿Cuáles pueden ser ejemplos de pruebas farmacogenéticas?
Actualmente existen diversas pruebas farmacogenéticas que pueden solicitarse. A continuación se muestran algunos fármacos para los cuales se dispone de pruebas farmacogenéticas.
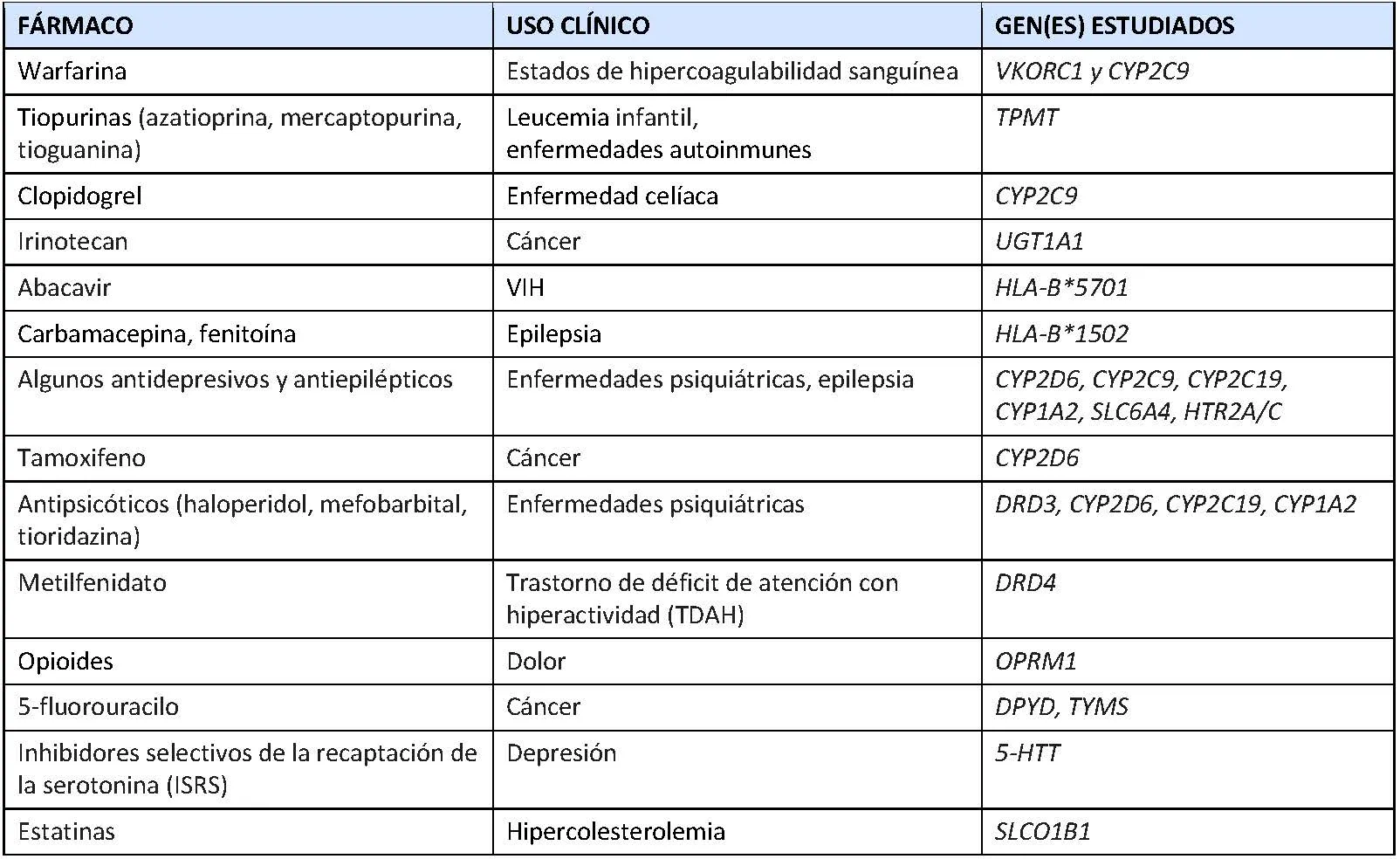
¿Deberían realizarse las pruebas farmacogenéticas a todo el mundo?
Actualmente sólo están indicadas si una persona va a tomar o está tomando un medicamento que tiene una prueba farmacogenética disponible.
¿Es indispensable realizar una prueba farmacogenética antes de tomar ciertos medicamentos?
No. En ciertos casos se puede recomendar realizar este tipo de pruebas, como en el caso del irinotecan, pero no es indispensable.
¿Por qué estas pruebas sólo se realizan una vez en la vida?
El material genético de una persona no cambia a lo largo de la vida. Sin embargo, existen muchas pruebas farmacogenéticas diferentes, por lo que si se toma otro medicamento puede ser que se realice otro estudio farmacogenético distinto.
¿Si se realiza la prueba farmacogenética se puede evitar la monitorización del fármaco?
No. Aparte de la genética, existen otros factores que pueden afectar a las concentraciones del fármaco, por lo que la monitorización del fármaco sigue siendo necesaria.
¿Qué tipo de muestra se utiliza?
La determinación se realiza a partir de una muestra de sangre venosa del brazo. También puede utilizarse una muestra de saliva o un frotis de la garganta, recogidos por raspado de la cara interna de la mejilla.
¿En qué se diferencian las pruebas farmacogenéticas del resto de pruebas genéticas?
Las pruebas farmacogenéticas se realizan para evaluar la potencial respuesta de una persona a un tratamiento farmacológico. La mayoría de pruebas genéticas se han desarrollado como ayuda en el diagnóstico o para predecir el desarrollo de una enfermedad genética, o bien para detectar bacterias y virus. También se pueden utilizar en medicina forense y para establecer relaciones de paternidad. Para más información, consultar el artículo sobre el universo de la genética.
¿La monitorización varía después de realizar una prueba farmacogenética?
En función de los resultados obtenidos, la monitorización del fármaco podría ser diferente, especialmente cuando se empieza a tomar la medicación, se cambia la dosis, o cuando se añade o se retira otra medicación.
¿Deberían realizarse estas pruebas a otros miembros de la familia?
Esta cuestión debe discutirse con el médico y con el resto de miembros de la familia. En algunos casos puede ser útil; en otros casos solo puede ser importante si ellos van a tomar el mismo tipo de medicamento. Los resultados de las pruebas farmacogenéticas constituyen una información útil que cualquier familiar debería compartir con el médico, junto con los antecedentes médicos de la familia.
¿Cuáles son los criterios para realizar este tipo de pruebas?
El médico suele tener en cuenta el diagnóstico del paciente, sus antecedentes de efectos adversos a los medicamentos, las opciones terapéuticas disponibles, y las pruebas disponibles. Las pruebas farmacogenéticas no están destinadas a ser utilizadas de forma aislada, sino en conjunto con el resto de hallazgos clínicos.
¿Hay algo más que debería saber?
Para la mayoría de fármacos, las pruebas farmacogenéticas no se solicitan de forma indiscriminada. Sin embargo, pueden estar indicadas cuando la medicación de interés tiene un margen terapéutico estrecho o está asociada con una tasa elevada de efectos secundarios.
El objetivo de las pruebas farmacogenéticas es ofrecer información adicional que permita seleccionar el tratamiento farmacológico y las dosis óptimas a administrar. Antes de someterse a una prueba farmacogenética se recomienda realizar asesoramiento genético y recibir y firmar un consentimiento informado.
Enlaces
Pruebas relacionadas:
Tiopurina metiltransferasa (TPMT)
Prueba de sensibilidad a la warfarina
Clopidogrel (genotipado de CYPC19)
Pruebas genéticas para el tratamiento dirigido del cáncer
Artículos:
Pros y contras de los estudios genéticos en la población
Farmacogenómica y efectos secundarios del tratamiento de la esquizofrenia
En otras webs:
MayoClinic: Medicina de precisión para el cáncer de mama
National Human Genome Research Institute (NIH): Farmacogenómica
Medline: Pruebas farmacogenéticas
Sociedad Española de Farmacogenética y Farmacogenómica (SEFF)
También conocido como: HSV-1, HSV-2, HHV1, HHV2, VHS, herpes oral, herpes labial, herpes genital
Nombre sistemático: virus del herpes simple tipo 1 y tipo 2
Aspectos generales
¿Por qué hacer el análisis?
Para hacer un cribado o un diagnóstico de la infección por el virus del herpes simple (VHS).
Pregúntenos














